近日,国际权威Top期刊Advanced Healthcare Materials(影响因子10.0,JCR一区Top,中国科学院SCI二区Top)以研究长文形式在线发表了我校化学化工学院杨美礼博士题为“Visualizing GSH-ONOO—Redox and TrackingLesion-Remedy of Acute Kidney Oxidative InjuryBased on a Dual-Site Chemosensor”的最新研究成果,我校为第一完成单位。
(Advanced Healthcare Materials, 2025, 14,)
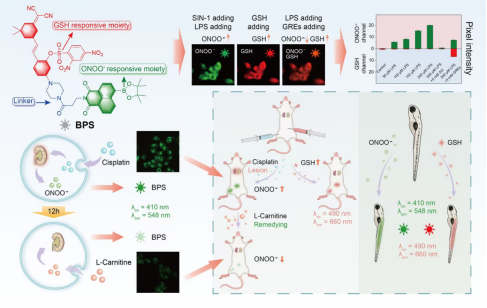
该研究报道了一种新型双位点荧光化学传感器(BPS),实现了药物性急性肾损伤(DIAKI)中过氧亚硝酸盐(ONOO⁻)与谷胱甘肽(GSH)的双通道实时监测,为氧化应激相关肾脏疾病的机制研究和治疗提供了创新工具。BPS通过独立激发/发射波长(ONOO⁻:410 nm/548 nm;GSH:490 nm/660 nm)实现两种生物标志物的同步精准检测,避免光谱重叠干扰。该传感器具有高灵敏度与选择性,检测限达181 nM(ONOO⁻)和2.42 μM(GSH),显著优于现有检测手段,并在复杂生物环境中展现强抗干扰能力。本研究首次在小鼠模型和HK-2细胞中实时追踪顺铂诱导的DIAKI病理进程及治疗恢复阶段,揭示ONOO⁻累积与GSH耗竭的时空调控规律,提出通过可视化GSH/ONOO⁻氧化还原平衡干预疾病进程的创新思路,为精准诊疗奠定基础。药物性急性肾损伤(DIAKI)是全球住院患者常见并发症,临床数据显示其死亡率高达30%-70%。传统检测方法依赖侵入性采样和延迟性生化指标,难以捕捉氧化应激动态变化。该研究报道的BPS传感器突破了这一瓶颈,首次证实DIAKI进程中ONOO⁻爆发性生成与GSH持续性耗竭的时空关联性,为靶向干预提供理论依据。在小鼠模型中验证了BPS对顺铂毒性及抗氧化剂治疗效果的实时评估能力,显著提升诊疗时效性。该传感器具备微创检测潜力,有望开发为无创试剂盒或植入式监测设备,推动床旁诊断(POCT)发展。(科研管理处、化学化工学院 文、图/周妮妮 审核/王晓玲、胡登卫)
文章链接:https://doi.org/10.1002/adhm.202500907